par Pierre-François Pradat
Département des Maladies du Système Nerveux
et Laboratoire UMRS 678, INSERM/UPMC,
Hôpital de la Pitié-Salpêtrière, Paris, France
Le 23e Congrès international sur la SLA a eu lieu à Chicago en décembre 2012.
Il a réuni de très nombreux spécialistes de la maladie qui sont venus présenter leurs travaux. Ce congrès a témoigné une nouvelle fois de la richesse de la recherche dans le domaine de la SLA, ce qui constitue une véritable source d’espoir pour les patients. Ce résumé traite des travaux qui concernaient des travaux de recherche clinique réalisés chez l’homme. Les travaux plus fondamentaux feront l’objet d’un autre compte-rendu.
1) Comment évaluer la progression de la maladie : la question du choix des meilleurs outils cliniques reste toujours un sujet d’actualité
On pourrait estimer qu’à l’heure des outils modernes de la biologie ou de l’imagerie, tout a été déjà dit sur les méthodes qui servent à mesurer l’évolution de la maladie en se basant sur des mesures cliniques. Ce serait se tromper car c’est une question qui n’est pas résolue et qui revêt une importance considérable et il faut bien admettre que les outils dont nous disposons actuellement sont insuffisants. Disposer de moyens fiables pour mesurer le stade d’évolution de la maladie est en effet essentiel à la fois pour le suivi des patients dans la pratique clinique mais également pour évaluer l’effet de nouveaux traitements.
Une étape importante avait été franchie à la fin des années 1990 où un consensus avait établi sur une échelle qui reflète le handicap lié à la maladie. Cette échelle appelée ALSFRS (Amyotrophic lateral sclerosis rating scale) établit un score qui prend en compte les différentes fonctions de la vie quotidienne qui peuvent être affectées par la maladie (l’écriture, la marche, l’habillage, la respiration notamment). Cette échelle est utilisée en routine par les neurologues et sert de base pour évaluer l’impact de nouveaux traitements sur la fonction motrice dans de nombreux essais thérapeutique. Toutefois, si elle établit une appréciation relativement fiable du handicap de la maladie en fournissant un score global, elle ne traduit pas directement son stade d’évolution au cours du temps. Créer une échelle qui répondrait à ce besoin est un exercice difficile car il s’agit d’une pathologie très hétérogène dans son mode de début, dans les parties du corps qui sont affectées par le déficit moteur et dans son rythme évolutif.
Deux équipes ont présenté de nouveaux systèmes de cotation qui prennent en compte cet aspect évolutif en définissant des stades successifs de la maladie. L’équipe anglaise d’Ammar Al Chalabi a présenté une échelle récemment publiée dans la revue Brain. Cette échelle comprend plusieurs stades qui prennent en compte deux aspects. Le premier est l’extension possible du déficit moteur dans les différentes parties du corps (stade 1: une première région, stade 2 : une deuxième région et stade 3 une troisième région. Le second aspect, et il s’agit là d’une originalité de cette échelle, est de prendre en compte le moment où sont décidées des interventions pour pallier à une atteinte nutritionnelle, par la réalisation d’une gastrotomie, ou respiratoire par la mise en route d’une ventilation au masque (stade 4). Cette nouvelle échelle a fait l’objet de validations statistiques sur la base de l’analyse des données cliniques issues de série importantes de patients. Cet outil a été présenté pendant le congrès et a fait l’objet d’un intérêt important de la part de la communauté des neurologues. La critique principale qui a été formulée est qu’il n’existe pas de consensus international sur les critères qui définissent le moment où les interventions sont décidées. C’est notamment le cas de la gastrotomie où il existe des différences de pratique importantes entre les centres, la décision de gastrotomie pouvant intervenir à des stades plus ou moins précoces. On comprend ainsi que cette hétérogénéité soit un obstacle à l’utilisation d’une telle échelle pour des essais thérapeutiques faisant intervenir plusieurs centres (« essais multicentriques »). Une seconde échelle établissant des stades successifs de la maladie a été présentée par Adriano Chio (Italie). Elle consiste à reprendre des catégories déjà prises en compte dans l’échelle ALSFRS mais à les regrouper en fonctions principales qui sont la capacité à communiquer, à se déplacer, à manger et à respirer. Le stade de la maladie est ensuite défini par le nombre de fonctions affectées (stade 0 : perte d’aucune de ces fonctions, stade 1 : perte d’une fonction, stade 2 : perte de deux fonctions…). Un des intérêts de cette échelle, au delà de sa simplicité puisqu’elle utilise des items déjà pris en compte dans l’ALSFRS, est probablement d’établir un meilleur reflet de la qualité de vie des patients. Il s’agit d’un point essentiel car il n’existe actuellement pas de consensus sur une échelle de qualité de vie dans la SLA. Il est en effet assez généralement reconnu que les échelles classiques et générales, utilisées indistinctement dans toutes les pathologies, ne sont pas adaptées au cas particulier de la SLA.
2) Les marqueurs neuroradiologiques de la maladie
Imagerie par PET-scan : mesurer l’inflammation dans la maladie
Si la sclérose latérale amyotrophique n’est pas une maladie primitivement inflammatoire, comme c’est le cas de la sclérose en plaques, on sait toutefois que des processus inflammatoires sont très probablement impliqués dans la progression de la maladie. C’est un aspect qui a été bien démontré dans des modèles animaux de la maladie. Les cellules qui sont responsables de l’inflammation dans la SLA, sont appelées cellules microgliales. Elles peuvent être dans un état de repos ou bien en réponse à une agression du système nerveux se convertir dans un état dit « activé » où elles produisent des molécules de l’inflammation.
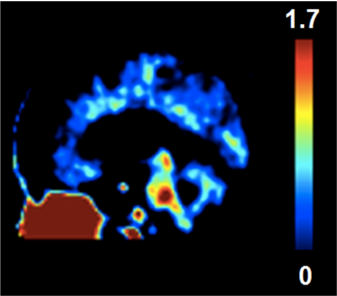
Figure 1 : PET-scan montrant les zones où le traceur radioactif se fixe sur les cellules microgliales dans le cerveau
Des études chez la souris avaient montré que cet état d’activation était associé à la progression de la maladie. L’étude présentée par Philippe Corcia (Tours) montre que cet état d’activation des cellules microgliales peut être visualisé chez l’homme (figure 1). Pour cela, son équipe a utilisé un outil appelé PET-scan. La base de cette méthode est d’injecter dans le sang des molécules marquées par un isotope radioactif (radiotraceurs) et de visualiser les régions du cerveau où ces molécules vont atteindre leurs cibles. Dans le cas présent, il s’agit d’un nouveau traceur qui se fixe sur les cellules microgliales lorsqu’elles sont activées. Grâce à cette technique, il était possible de visualiser les régions où le processus inflammatoire était actif, principalement les zones motrices. Cet outil pourrait s’avérer extrêmement utile pour évaluer l’effet de traitements neuroprotecteurs visant à diminuer les processus inflammatoires
L’IRM : un marqueur de l’évolution de la maladie
Léonard Van den Berg (Hollande) a présenté une étude sur la mesure en IRM de l’épaisseur du cortex cérébral chez 112 patients souffrant de SLA. Cette étude révèle qu’il existe une corrélation entre cette mesure et le score fonctionnel des patients mesuré par l’échelle ALSFRS-R.
L’imagerie de la moelle épinière est particulièrement intéressante dans une pathologie dont une caractéristique principale est de toucher les cornes antérieures de la moelle où sont situés les corps cellulaires des motoneurones. Elle présente des difficultés techniques importantes en raison du faible diamètre de cette structure (environ un centimètre), de l’interférence des mouvements physiologiques (respiration, battements cardiaques ou encore déglutition) et de la présence d’artéfacts liés à la proximité de la moelle avec les structures osseuses, discales et le liquide céphalo-rachidien. Avec les progrès de l’imagerie, ces problèmes parviennent à être de mieux en mieux contrôlés.
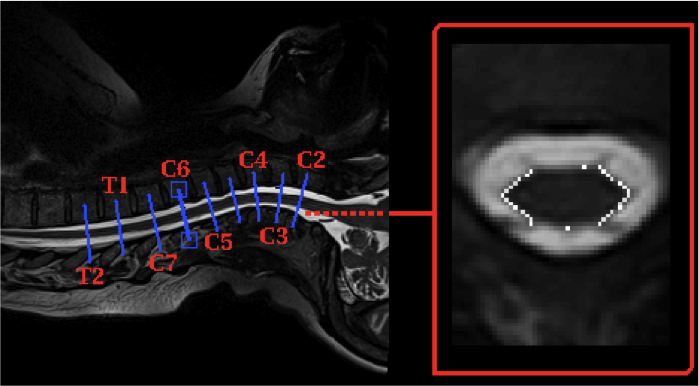
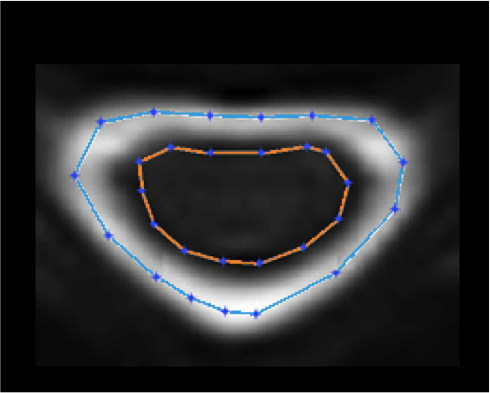
Un travail présenté par Pierre-François Pradat (Paris) utilisait une méthode permettant de mesurer avec précision la surface de la moelle épinière (figure 2). Cette méthode s’est révélée être suffisamment sensible pour détecter une diminution du volume de la moelle épinière chez les patients par rapport à des sujets indemnes de SLA. Lorsque cette IRM était répétée chez les patients après un délai moyen de 11 mois, il était possible de mesurer une diminution du diamètre de la moelle qui était corrélée à l’aggravation clinique de la maladie. Cette étude suggère donc que la mesure de l’atrophie de la moelle pourrait constituer un marqueur de l’aggravation de la maladie, pouvant potentiellement être utilisée pour mesurer l’effet de médicaments neuroprotecteurs.
Figure 2 : IRM de la moelle épinière au niveau cervical. Il est possible d’extraire des coupes transversales de la moelle épinière. Grâce à des logiciels de traitement de l’image, on mesure la surface de la moelle épinière (d’après Pradat et al, 2012)
3) Essais thérapeutiques
Les résultats de plusieurs essais thérapeutiques ont été présentés lors du meeting.
Ceftriaxone : agir contre l’excès de glutamate
Une étude nord-américaine avait été menée afin de tester une molécule initialement utilisée comme antibiotique, la ceftriaxone. Ce candidat thérapeutique avait été sélectionné par une approche dite de criblage de molécules («drug screening »). Cette méthode consiste à tester un nombre important de molécule dans un modèle in vitro afin de sélectionner celles qui peuvent modifier une voie qu’on pense impliquée dans la maladie. Dans le cas présent, il s’agissait d’identifier des molécules qui pouvaient augmenter la recapture du glutamate. On pense en effet qu’un excès de glutamate est impliqué dans la physiopathologie de la maladie (c’est d’ailleurs sur la base de cette hypothèse qu’a été développé le riluzole qui est un anti-glutamate). Il est ressorti de ce processus de criblage que la ceftriaxone possédait cette activité d’augmenter la recapture du glutamate par les cellules environnantes (les astrocytes) et donc de limiter sa toxicité pour les motoneurones. Malheureusement, les résultats de l’essai qui a été présenté par le Meritt Cudkowitz (Boston, USA) ne confirment pas que cette molécule apporte un bénéfice clinique chez les patients. Cette étude, qui a inclus un nombre important de sujets (513 sujets dont 340 traités par ceftriaxone et 173 par un placebo) n’a montré aucun effet sur les différents critères cliniques testés.
Olesoxime : un essai négatif mais qui fournit des informations importantes
Les résultats finaux de l’essai thérapeutique avec l’olesoxime ont été présentés par Timothée Lenglet (Paris).
Cette molécule avait démontré un effet neuroprotecteur sur plusieurs modèles de maladies neurodégénératives et en particulier sur le modèle murin le plus répandu de la SLA (des souris qui expriment une mutation sur le gène SOD1, mutation qui est responsable de rares formes familiales de SLA). L’olesoxime interagit avec la fonction des mitochondries. Les mitochondries sont considérées comme les « centrales énergétiques » de la cellule et leur dysfonctionnement semble jouer un rôle clé dans la pathogénie de la SLA. Il s’agissait d’une étude multicentrique. Au total 512 patients ont été inclus dans un essai randomisé en double aveugle dans lequel les patients prenaient l’olesoxime ou le placebo en plus de leur traitement par riluzole. L’étude s’est révélée négative pour l’ensemble des critères étudiés en dehors d’un effet marginal sur l’échelle fonctionnelle de la SLA (ALSFRS) à 9 mois, un effet qui est toutefois trop faible pour avoir un impact significatif sur la fonction des patients. Un enseignement important est que la survie globale des patients inclus dans l’étude était sensiblement supérieure à celle mesurée dans les essais thérapeutiques passés. Cela souligne sans doute par ailleurs les progrès accomplis ces dernières années dans la prise en charge symptomatique de nos patients SLA que ce soit sur un plan nutritionnel ou respiratoire avec en particulier l’usage plus étendu de la ventilation non invasive.
NP001 : agir contre l’activation des macrophages
Il s’agit d’une stratégie thérapeutique qui vise à luter contre l’inflammation. Nous avons vu précédemment, qu’un des acteurs majeurs du déclenchement de processus inflammatoires dans le système nerveux reposait sur les cellules microgliales qui résident normalement dans le système nerveux et qui peuvent s’activer en réponse à divers stimuli. Un autre mécanisme, qui a été défendu par Stanley Appel (USA) sur la base de travaux fondamentaux, est que des cellules présentes dans le sang et impliquées dans l’inflammation, les macrophages, puissent également s’activer et envahir le système nerveux central. La molécule NP001, des laboratoires Neuraltus, par des mécanismes qui ne sont pas complètement élucidés, vise à bloquer ce processus. Robert Miller (USA) a présenté les résultats d’une étude de phase II où le produit était administré par voie intraveineuse tous les mois pendant 6 mois. Une série de 136 patients étaient divisés en 3 groupes (placebo, NOP001 à faible dose, NP001 à fortes doses). L’analyse a montré qu’il existait peut être une tendance à l’amélioration de paramètres cliniques. Il faut toutefois souligner que le nombre de patients était faible, la durée d’observation courte et donc qu’il est impossible de tirer des conséquences définitives de ce résultat. Une étude de phase III est prévue en 2013 pour poursuivre l’analyse des effets de cette molécule.
CK2017357 (Tirasemtiv) : améliorer la contraction musculaire
Cet essai se situe dans une approche originale puisqu’il s’agit non plus d’agir sur le motoneurone lui-même mais sur le muscle. Lors du précédent congrès avaient été présentés les résultats préliminaires d’une étude visant à bloquer une protéine, la protéine Nogo-A, qui est en excès dans le muscle de patients SLA et pourrait nuire à la réinnervation du muscle (Pierre-François Pradat et al, 2011). Cette étude ayant montré une très bonne tolérance du traitement, une étude internationale de phase II contre placebo va débuter en 2013 pour évaluer si des perfusions bimensuelles d’anticorps anti-Nogo-A permettent de ralentir le déclin moteur lié à la maladie. L’étude présentée lors du congrès par Jeremy Shefner(USA) a un objectif différent. Il s’agit en effet d’agir directement sur les capacités de contraction du muscle en activant une protéine musculaire appelée troponine. Ce travail regroupait des données provenant de trois essais antérieurs menés avec le Tirasemtiv (laboratoires Cytokinetics) qui chacun avait des effectifs de patients limités. Les résultats sont encourageants car il existe peut être un effet (« une tendance ») pour une amélioration de scores cliniques comme la force ou l’endurance. A noter que ce traitement, par une interaction pharmacologique, augmentait les taux de riluzole lorsque ce traitement était associé. Cela justifie qu’en cas d’association les doses de riluzole soient diminuées de moitié. Une étude de phase II, avec un nombre de patients plus important, permettra de dire si ces résultats sont confirmés. L’étude nommée BENEFIT ALS (pour Blinded Evaluation of Neuromuscular Effects and Functionnal Improvement with Tirasemtiv in ALS) est une étude multinationale qui sera menée aux Etats Unis, au Canada et dans plusieurs pays Européens dont la France.
Les anti-sens dans les formes familiales de SLA liées à une mutation de la protéine SOD1
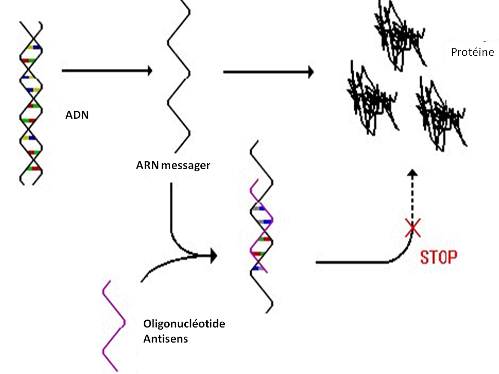
Le gène SOD1 a été le premier gène qui a été identifié dans certaines formes familiales de SLA. En dépit d’intenses recherches, utilisant notamment des modèles animaux générés à partir de cette anomalie génétique, on ne connaît toujours pas les mécanismes exacts en cause. Même en l’absence de ces connaissances, des stratégies qui viseraient à bloquer l’expression du gène anormal restent tout à fait pertinentes. Une de ces stratégies a été présentée par Timothy Miller (USA) et repose sur l’utilisation d’oligonucléotides antisens. Il s’agit de petites séquences d’acides nucléiques, les composants de l ‘ADN qui ont pour effet d’empêcher la formation de l’ARN messager et donc au total de la protéine correspondante.
Figure 3 : Mécanisme d’action des oligonucléotides anti-sens : bloquer la production de la protéine SOD1 en se liant aux ARN messager
Comme il s’agit d’une thérapeutique innovante, sans recul sur ses effets toxiques possible, un long parcours d’études d’abord précliniques chez l’animal puis de façon très prudente dans des petites séries de patients, avec des doses très bien contrôlées, a été nécessaire. Pendant le congrès Timothy Miller a présenté des premiers résultats sur une série de 32 patients présentant une forme de SLA liée au gène SOD1. Le traitement était administré directement dans le liquide céphalo-rachidien (voie intrathécale). Deux résultats importants ressortent de cette étude. Le premier est que le traitement est très bien toléré. Le second est que les oligonucléotides étaient détectables aux doses attendues dans le liquide céphalorachidien. En revanche, aucun résultat n’a été communiqué sur l’effet du traitement sur l’évolution de la maladie.
Injection de cellules souches dans la moelle épinière
Les thérapeutiques basées sur l’utilisation de cellules souches suscitent un espoir important pour les patients. Les incertitudes sur les méthodes à employer (types de cellules, voies et modalités d’injections …) et les dangers potentiels importants (formation de tumeur à long terme notamment, lésions nerveuses provoquées par les procédures d’injection…) imposent que les premiers essais soient menés de façon prudente. Cette lenteur des avancées est parfois ressentie comme une frustration par les patients. Il est important d’expliquer que des essais trop précipités pourraient conduire à des effets secondaires graves susceptibles d’entraîner une suspension des essais dans ce domaine pendant de nombreuses années. Il existe le précédent dans le domaine de la thérapie génique où lors des premiers essais des complications graves inattendues, ont au total ralenti l’évolution dans ce domaine en créant une suspicion générale sur le bien fondé de cette approche. Des premiers résultats d’un essai mené par la société de biotechnologie Neurastelm ont été présentés par Jonathan Glass (USA). Cet essai a concerné 18 patients parmi lesquels l’injection a été réalisée dans la moelle lombaire dans 12 cas et la moelle cervicale dans 6 cas. L’injection était réalisée par un neurochirurgien très expérimenté dans la chirurgie de la moelle épinière et un film de l’intervention a été présenté pendant le congrès. Il a été notamment montré l’attention qui devait être portée par le chirurgien pour ne pas léser les vaisseaux qui irriguent la moelle épinière, en raison du risque de créer un hématome dont les conséquences seraient catastrophiques. Le résultat principal de cette étude est que la procédure n’a pas entraîné de complications post-chirurgicales. Les courbes d’évolution des patients ont été présentées lors du congrès sans qu’il soit possible de conclure sur une efficacité ou non du procédé. En effet si certains patients semblaient avoir une évolution relativement stable, il était impossible de déterminer s’il s’agissait de l’évolution naturelle de la maladie ou bien d’un effet bénéfique du traitement. Il aurait été souhaitable de disposer d’informations sur le profil général d’évolution de la maladie avant l’intervention. Des échantillons de moelle épinière ont pu être analysés chez quelques patients. Il a pu être constaté que la procédure d’injection n’entraînait pas de lésions significatives de la moelle épinière. Par ailleurs, des cellules provenant du donneur étaient retrouvées, prouvant bien que l’injection avait été efficace. En revanche il est à regretter qu’aucunes données n’aient été présentées sur le devenir de ces cellules et notamment leur degré de différenciation.
4) Traitements symptomatiques
Un travail collaboratif réalisé à Pitié-Salpêtrière, sous la direction de Pierre-François Pradat, et les Etats-Unis, sous la direction de Benjamin Brooks, a été présenté sur l’évaluation de l’hypersalivation dans la SLA. Il s’agit d’un symptôme fréquent, extrêmement gênant pour les patients et qui pourtant a fait l’objet de peu d’études. Des possibilités thérapeutiques existent mais pour les évaluer il est indispensable de disposer d’une échelle fiable. Dans ce travail présenté par Maya Abdelnour (Paris), et qui vient récemment d’être publié, deux échelles adaptées spécifiquement à la mesure de l’hypersalivation ont été évaluées sur une série importante de patients. Une analyse statistique a montré que ces échelles permettaient une mesure sensible et fiable de l’hypersalivation. C’est d’ailleurs l’une des ces deux échelles appelée SSS («sialorrheascoringscale ») qui a été utilisée pour l’évaluation de l’effet de la radiothérapie pour diminuer l’hypersalivation dans la SLA dans le travail présenté par Avi Assouline et Pierre-François Pradat (voir l’interview d’Avi Assouline)
5) Nutrition et épidémiologie
Le rôle des habitudes alimentaires avant la survenue de la maladie ?
On connaît l’importance du maintien d’un bon équilibre nutritionnel lorsque la SLA est installée. La perte de poids est notamment un facteur associé à l’évolutivité de la maladie et est un paramètre qui doit faire l’objet d’une surveillance attentive. Le rôle éventuel de facteurs nutritionnels dans l’apparition de la maladie reste inconnu. Une étude présentée par M Seelen (Hollande) a porté sur un interrogatoire nutritionnel réalisé chez 747 patients souffrant de SLA comparés à 2385 sujets indemnes de la maladie (sujets « contrôles »). Les sujets devaient préciser leurs habitudes nutritionnelles avant la survenue de la maladie. Les auteurs de ce travail rapportent que les sujets qui allaient développer une SLA avaient statistiquement une alimentation plus riche en matières grasses et en nutriments ayant des propriétés antioxydantes. Il n’y avait en revanche pas de relation avec la consommation de glutamate ou de calcium. Ce type d’étude doit être interprété avec prudence compte tenu de la multiplicité des facteurs analysés. Elle nécessite d’être confirmée par d’autres études.
La vitamine D : un nouveau facteur impliqué dans la SLA ?
Une étude importante sur le rôle possible d’une carence en vitamine D a été présentée par Nicolas Pageot qui appartient à l’équipe de William Camu (Montpellier). On sait que la vitamine D est un modulateur de l’immunité. Les auteurs ont réalisé une étude rétrospective de janvier 2010 à décembre 2011 et ont identifié 74 patients pour lesquels un dosage de vitamine D était disponible. Le résultat de cette étude est qu’en présence d’un déficit sévère en vitamine D, la maladie évolue 6 fois plus vite qu’en cas de dosage normal. Nicolas Pageot a insisté sur le fait que ces résultats devaient être confirmés par une étude prospective dans laquelle un dosage de vitamine D sera réalisé systématiquement chez les patients. Il n’y a pas actuellement suffisamment d’arguments pour préconiser de façon systématique la prise de vitamine D chez les patients souffrant de SLA.
Analyser des foyers d’incidence élevée de SLA
L’étude épidémiologique permet de déterminer le nombre de patients atteints SLA dans une région, et de géo localiser les patients. Des zones géographiques de sur-incidence de la maladie ou isolats ou clusters sont ainsi dépistées. Dans ces zones géographiques particulières, des hypothèses environnementales peuvent être testées. Dans une communication présentée par Emmeline Lagrange, l’équipe de Grenoble et de Montpellier a rapporté l’étude d’un village identifié en Haute Savoie où l’hypothèse d’une toxine sécrétée par des cyanobactéries a été étudiée avec des prélèvements d’eau, de mousse mais aussi par détection positive dans un cerveau d’une toxine appelée BMAA. On rappelle que cette hypothèse toxique est actuellement évoquée pour rendre compte de l’incidence particulièrement élevée de SLA dans l’île de Guam.
Interview du Dr Lenglet sur les nouveautés en électrophysiologie
Le Dr Lenglet est neurologue à l’hôpital de la Salpêtrière et travaille également dans l’unité de neurophysiologie de la Pitié-Salpêtrière. Il répond à quelques questions sur les nouveautés dans le domaine de l’électrophysiologie.
Dr Pradat : que pensez vous du niveau global des communications dans le domaine de la neurophysiologie. Est-ce un domaine actif ?
C’est clairement un domaine actif. Alors que les communications l’année passée portaient largement sur la contribution de l’électroneuromyogramme standard (EMG) pour le diagnostic de SLA (nouveaux critères d’Awaji), cette édition 2012 était marquée par la présentation de différentes techniques de neurophysiologie (potentiels évoqués moteurs, EMG de fibre unique, comptage d’unité motrice…) comme marqueurs de progression de la pathologie, au même titre que l’imagerie par exemple.
Dr Pradat : On a beaucoup parlé des techniques de comptage des unités motrices durant ce congrès. Pourriez-vous nous expliquer simplement le principe ?
Le nerf périphérique moteur peut se décrire comme un faisceau d’axones reliant chacun un neurone moteur à plusieurs fibres musculaires (unité motrice). L’étude de conduction motrice effectuée en routine dans le cadre de l’EMG standard mesure des potentiels d’action global musculaire (PAGM) correspondant à la mise en jeu de l’ensemble des unités motrices disponibles mais sans refléter leur nombre, or l’on sait que dans la SLA des mécanismes de compensation (réinnervation collatérale à partir des fibres nerveuses restantes) permettent le maintient de PAGM normaux en dépit d’une baisse importante des unités motrices fonctionnelles. Le comptage d’unité motrice introduit il y a une quarantaine d’année par Mc Comas permet à partir de techniques de stimulations progressives à très basses intensités ou de méthodes statistiques d’évaluer la taille moyenne et le nombre effectif des unités motrices contribuant au PAGM.
Dr Pradat : Pouvez vous nous parler des principaux résultats qui ont été présentés dans ce cadre ?
Je retiens la communication de C. Neuwirth et al. (Muskelzentrum / ALS Clinic, Cantonal HospitalSt.Gallen, Switzerland) portant sur le suivi longitudinal d’une trentaine de patients SLA issus de 3 centres européens via une nouvelle technique de comptage d’unité motrice appelée MUNIX. Les résultats obtenus étaient comparés à ceux de marqueurs de progression classiques de la pathologie telle que l’échelle fonctionnelle ALSFRS-r. Des variations significatives du comptage d’unité motrice étaient enregistrées dans plusieurs territoires après seulement quelques mois de suivi (6-9 mois) en l’absence à ce stade de baisse significative de l’échelle fonctionnelle. De tels résultats ont déjà été rapportés avec d’autres techniques de comptage d’unité motrice mais ce qui est nouveau c’est qu’ils sont ici obtenus via une technique très simple d’emploi, bien tolérée par le patient, dont le temps de réalisation n’excède pas 5-10 minutes et donc très simplement utilisable en routine. Le tout suggère l’intérêt potentiel d’une utilisation systématique de la technique comme marqueur de progression de la SLA dans le contexte d’essais thérapeutiques par exemple.
Dr Pradat : L’usage indique que le comptage d’unité motrice demeure relativement confidentiel, comment pensez vous que cette technique puisse s’imposer ?
Le frein à l’essor du comptage d’unité motrice était principalement lié à la multitude des techniques disponibles et à l’absence de consensus sachant par ailleurs que bon nombre d’entre elles sont difficilement utilisables en routine. On retient à ce titre que les MUNIX font partie d’un vaste programme européen (projet SOPHIA, coordonnateur L. Van Den Berg, Utrecht) visant à une harmonisation progressive des pratiques concernant différents biomarqueurs de la SLA, ce qui lui permettra peut être de s’imposer comme une technique de référence dans les principaux centres SLA européens.
Interview du Dr Avi ASSOULINE
Le Dr Avi Assouline, oncologue et radiothérapeute (Centre Clinique de la Porte de Saint Cloud), et le Dr Pierre-François Pradat, neurologue, ont établi une collaboration pour développer un protocole d’étude du traitement de l’hypersalivation basé sur la radiothérapie des glandes salivaires. Ils ont présenté leurs travaux lors du dernier congrès sur la SLA à Chicago début décembre 2012.
Question 1: On connaît l’utilisation de la radiothérapie dans les cancers, pouvez-vous nous expliquer en quoi elle peut être adaptée pour traiter l’hypersalivation ?
Réponse : Le point de départ est de se servir d’un effet secondaire délétère de la radiothérapie dans le cadre du traitement des cancers de la cavité buccale qui est l’hyposialie (la diminution – souvent importante – de la quantité de salive). Il est possible d’utiliser cet effet négatif chez des patients cancéreux en un effet « positif » chez des patients, qui eux, pour diverses raisons, ont « trop » de salive. Ce qui est le cas de nombre de patients atteints de maladie neurologique dont les patients atteints de la SLA. Permettez moi de rendre hommage à une autre radiothérapeute, le Dr Sylvie Delanian, qui la première, a commencé à travailler sur ce processus, avec le Dr Pradat.
Question 2 : Pouvez-vous nous expliquer en quoi consiste ce traitement en pratique ?
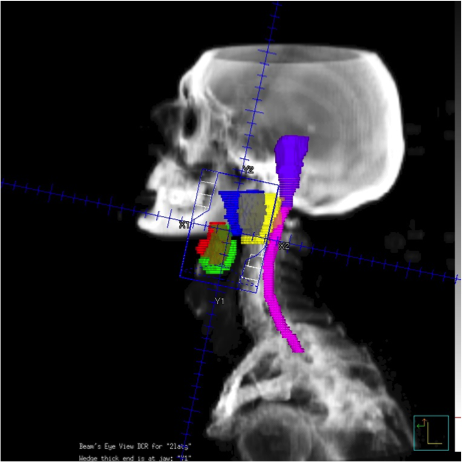
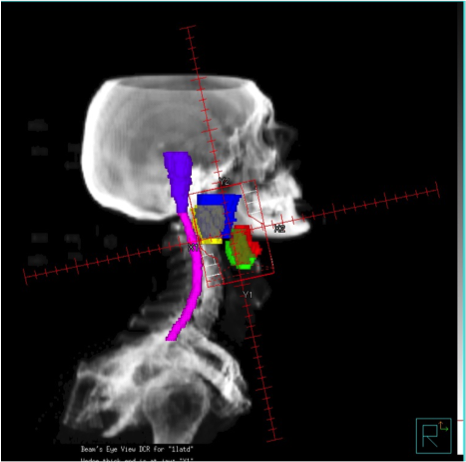
Réponse : Le principe est d’irradier les glandes principales qui produisent la salive que sont la glandes parotides et les glandes sous-maxillaires afin d’en diminuer le fonctionnement. Nous utilisons pour cela les nouvelles techniques de radiothérapie à notre disposition pour permettre de cibler précisément la région à irradier ce qui permet également d’épargner au maximum l’irradiation des organes de voisinage et donc d’avoir un maximum d’efficacité avec un minimum d’effets secondaires. Pour cela, le patient va bénéficier d’un scanner dit de repérage dans le Centre de Radiothérapie et durant ce scanner, on lui fabriquera un masque de contention qui permet de maintenir la tête du patient dans la bonne position durant le traitement. C’est sur ce scanner qu’ensuite, le plan de traitement du patient sera établi de façon personnalisée. Ce travaille implique la collaboration du radiothérapeute et d’un radio-physicien (physicien spécialiste des rayons X travaillant dans le Centre de Radiothérapie). En fonction de certains critères, le plan de traitement comprendra soit 2 séances (sur 3 jours), soit 4 séances (sur 10 jours).
Figure : Représentation sur une image reconstruite en 3D des 2 champs d’irradiation (virtuels) : petits rectangles, en bleu (figure à gauche) et en rouge (figure à droite) avec à l’intérieur de ces champs, les 4 principales glandes salivaires (parotides droite et gauche et glandes sous-maxillaires droite et gauche). Juste à coté, la moelle épinière (en rose) et le tronc cérébral (en violet) sont représentés mais sont totalement exclus des champs de radiothérapie
Question 3 : Quelle était l’efficacité de ce traitement dans le travail que vous avez présenté
Réponse : L’efficacité, sur les 40 premiers malades de l’étude (et avec un recul d’au moins 3 mois pour chaque malade) a été nette. Sur les 40 malades, 32 ont eu une réponse estimée complète, c’est-à-dire qu’ils sont passés d’un état de gêne très important avec souvent une salive qui coulait sur les vêtements, les objets environnants, à une disparition complète de la gêne salivaire. Les 8 autres patients ont également tiré un bénéfice de la radiothérapie avec une réduction significative de la gêne mais de manière moins spectaculaire.
Question 4 : Avez-vous observé des effets secondaires importants
Réponse : Sur les 40 patients traités dans l’étude présentée au congrès, seuls 15 d’entre eux ont présentés des effets secondaires pendant la radiothérapie. Il s’agissait soit d’une sècheresse buccale (mais qui paradoxalement traduit aussi chez ces patients une « trop grande » efficacité de la radiothérapie soit une salive plus épaisse, soit de douleurs oro-pharyngées, ou d’une modification du goût. Mais ces effets ont à chaque fois été d’intensité très modérée, ne gênant le patient que durant quelques heures à quelques jours après la radiothérapie, ne nécessitant aucun traitement (ou juste la simple prise de doliprane si douleurs), et toujours transitoires, disparaissant très rapidement.
Question 5 : il s’agissait de résultats préliminaires, pouvez-vous nous dire qu’elles seront les prochaines étapes du travail que vous menez avec le Dr Pierre-François Pradat ?
Réponse : Nous avons déjà présenté, avec le Dr Pradat, nos résultats préliminaires à 2 congrès importants (le congrès de la Société Française de Radiothérapie Oncologique à Paris en 2011 et le congrès sur la SLA à Chicago début décembre 2012). Ces résultats préliminaires sont maintenant arrivés à un stade plus avancé, avec plus de patients traités (50 patients), et un plus grand recul dans la surveillance. Les résultats définitifs seront soumis à une revue scientifique internationale, ce qui aura pour impact de diffuser plus largement encore nos résultats et surtout la technique de traitement à d’autres équipes dans le monde et ce qui permettra enfin à plus de patients, notamment en France où cette indication de radiothérapie est méconnue, de pouvoir en bénéficier.