La fondation Thierry Latran remercie vivement le Dr Pierre-François Pradat qui nous résume ce congrès.
Dr Pierre-François Pradat
Hôpital de la Pitié-Salpêtrière, laboratoire de recherche INSERM U678 (Dr Habib Benali)
Le dernier congrès de l’ENCALS a eu lieu du 31 mai au 2 juin 2013 dans la ville de Sheffield en Grande Bretagne. L’ENCALS (European Network for the cure of ALS) est un réseau européen qui rassemble cliniciens et chercheurs s’intéressant à la SLA dans le but de favoriser les échanges et les collaborations. Dans ce résumé nous n’aborderons pas l’ensemble des différents thèmes évoqués mais nous avons sélectionné, avec une part nécessairement subjective, quelques aspects qui nous ont semblé particulièrement novateurs et intéressants.
1) C9ORF72 : un gène impliqué dans la SLA mais un rôle toujours mystérieux
La SLA dans la très grande majorité des cas n’est pas familiale. L’étude des formes familiales rares est un axe de recherche essentiel, sachant que les mécanismes en jeu ont certainement des points communs avec les formes non familiales. On savait depuis 2006 qu’un gène situé le chromosome 9 pouvait être responsable de cas familiaux de SLA associées à des troubles intellectuels, ce qui est inhabituel dans cette maladie. De nombreuses équipes internationales se sont alors engagées dans la quête du gène responsable situé dans cette région du chromosome. C’est finalement en 2011, qu’est venue la découverte majeure de l’implication d’un gène au nom compliqué, le gène C9ORF72. L’anomalie génétique est inhabituelle et c’est la raison pour laquelle il a fallu autant de temps pour la détecter. Il s’agit de la répétition de six bases (les constituants élémentaires de la molécule d’ADN) qui ont la particularité de se situer dans des régions non codantes du gène. Depuis, de nombreux travaux, dont plusieurs ont été présentés à l’ENCALS visent à comprendre les anomalies qu’entraîne cette modification du gène C’est une question qui n’est absolument pas résolue actuellement. Notamment, la fonction normale du gène C9ORF72 n’est pas connue. Une conséquence de la modification du gène pourrait être une perturbation des ARN (les molécules synthétisées à partir de l’ADN e t qui serviront de matrice pour la synthèse des protéines). On citera notamment les travaux présentés par Steven Boeynaems (Belgique) où l’anomalie a été introduite dans un modèle de SLA chez le poisson zèbre (ce modèle est très utilisé car il se prête facilement aux manipulations génétiques et l’analyse des conséquences est plus simple que chez la souris). Ces travaux sont à rapprocher de ceux de l’équipe d’Edor Kabashi (Hôpital de la Salpêtrière) qui viennent d’être publiés dans la revue Annals of Neurology. Dans ce travail, les auteurs ont montré que les poissons zèbres déficients pour le gène C9ORF72 développaient des troubles moteurs. Il s’agit toutefois d’un modèle éloigné de l’homme et beaucoup d’espoirs sont fondés dans la mise au point future d’un modèle chez la souris.
2) L’électrophysiologie dans la SLA : un outil précieux pour comprendre les modifications des circuits neuronaux dans la moelle épinière
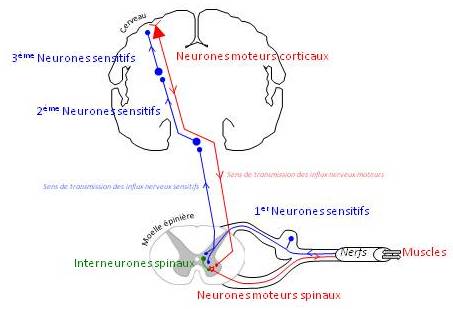
Il y eu ces dernières années des progrès importants dans le domaine de la biologie cellulaire et de la génétique. Il faut souligner que la compréhension des circuits neuronaux qui sont altérés dans la SLA a également une importance capitale pour comprendre la maladie et mettre au point de nouveaux traitements. Notamment, a été évoqué récemment le rôle d’autres populations de neurones. Les neurones moteurs reçoivent en effet un nombre considérable d’influx nerveux provenant d’autres cellules neuronales, comme les neurones sensoriels ou les interneurones. Des perturbations de ces influx pourraient engendrer des modifications des propriétés électriques et du fonctionnement des neurones moteurs. L’électrophysiologie fournit justement un moyen chez l’homme d’explorer ces modifications. L’atteinte des voies sensorielles avait été montrée grâce à l’IRM par un travail réalisé dans le laboratoire d’Habib Benali à la Salpêtrière par les Drs Pierre-François Pradat et Julien Cohen-Adad. En utilisant une méthode nouvelle d’électrophysiologie, l’équipe du Dr Véronique Marchand-Pauvert a pu montrer que cette atteinte sensorielle modifiait le fonctionnement des neurones moteurs lors d’une présentation faite par le doctorant Sina Sangari.
Figure 1 : les neurones moteurs reçoivent des influx nerveux (« afférences ») provenant d’autres neurones comme les neurones sensitifs ou des interneurones. Le fonctionnement correct des neurones moteurs est dépendant de l’intégration de ces différentes informations. Les Dr Marchant-Pauvert et Pradat analysent la perturbation de ces mécanismes d’intégration en utilisant à la fois des techniques d’imagerie et d’électrophysiologie
Il s’agit donc d’une voie de recherche prometteuse qui tire profit de méthodes avancées d’électrophysiologie qui peuvent s’appliquer à la fois chez l’homme et chez l’animal. Justement, des travaux ont été réalisés chez la souris par l’équipe du Dr Daniel Zytnicki (Paris) qui vont dans le sens également de l’implication d’autres populations de neurones que les neurones moteurs. Nicolas Delestrée a ainsi montré que les propriétés électriques des neurones moteurs n’étaient pas modifiées. En revanche, les influx nerveux provenant d’autres neurones sont susceptibles de modifier le fonctionnement des moteurs et peut-être induire leur dégénérescence.
3) L’inflammation dans la SLA : un rôle forcément négatif ?
Le rôle des cellules microgliales a été mis en avant grâce notamment aux travaux réalisés chez l’animal par le Dr Séverine Boilée (Hôpital de la Salpêtrière, Paris) et récemment chez l’homme, grâce à des travaux d’imagerie conduits par le Pr Philippe Corcia (Tours). Ces cellules, qui sont responsables de la réaction inflammatoire dans le système nerveux, seraient impliquées comme un facteur d’aggravation plus que de déclenchement de la dégénérescence motoneuronale. Ces cellules pourraient libérer des médiateurs inflammatoires toxiques pour les motoneurones. Toutefois, la situation pourrait être plus compliquée, cette inflammation étant susceptible d’avoir un rôle initialement protecteur dans les phases précoces de la maladie. On comprend aisément qu’une analyse précise de la succession des étapes d’inflammation, et de leur conséquence sur la viabilité des motoneurones, est nécessaire dans l’optique d’application de traitements anti-inflammatoires chez les patients. En dehors des cellules inflammatoires directement situées dans le système nerveux, les lymphocytes circulants pourraient également jouer un rôle. Ce fut l’objet d’une conférence donnée par Stanley Appel (USA) qui est à l’origine de nombreux travaux sur le rôle de l’inflammation et de l’immunité dans la SLA.
4) un chercheur français à l’honneur
Cette année, c’est le Dr Luc Dupuis qui a reçu le prix qui récompense un jeune chercheur pour des travaux de recherche marquants dans le domaine de la SLA. Le Dr Luc Dupuis travaille dans le laboratoire INSERM U1118 situé à Strasbourg et qui est dirigé par le Dr Jean-Philippe Loeffler.
Interview du Dr Luc Dupuis par le Dr Pierre-François Pradat
Tes travaux ont été les premiers à souligner le rôle central d’anomalies du métabolisme dans la SLA. Peux-tu nous expliquer ce qui t’a mis sur cette piste chez la souris ?
Nous avons constaté que nos souris modèles de SLA étaient plus maigres que les contrôles. Cela avait été publié plusieurs fois avant nos travaux, mais jamais personne ne s’était encore posé la question de la raison de cette anomalie. Cette maigreur de nos animaux transgéniques ne vient pas d’une perte d’appétit. Au contraire ces souris mangent plus que leurs contrôles. En fait, pour réaliser la même activité, les souris atteintes de SLA dépensent plus de calories.
Est ce que ces anomalies métaboliques jouent un rôle dans le déficit moteur ?
Oui, et pour le montrer, nous avons simplement nourri les souris avec des croquettes enrichies en graisses. Ce régime alimentaire a compensé la perte de poids, et plus important a augmenté la survie et retardé la progression de la maladie.
Tu as publié des travaux importants sur les anomalies du métabolisme lipidique chez l’homme. Finalement, est ce que l’on peut parler d’un effet protecteur des lipides ?
Chez la souris, certainement. Chez le patient, nous ne pouvons pas encore l’affirmer. Nous avons montré que les patients qui ont plus de lipides dans le sang ont une survie plus longue. D’autres ont confirmé ces travaux et ont montré que les patients en léger surpoids progressaient moins rapidement que les patients minces. Cependant, nous n’avons montré aucune relation de cause à effet pour le moment.
Nous savons, dans notre pratique neurologique courante que le contrôle du poids est un objectif majeur. Le fait que la perte de poids soit un facteur de mauvais pronostic est étayé par de nombreuses études. Tes travaux laissent penser qu’il serait sans doute prometteur d’agir de façon encore plus ciblée sur le métabolisme. Il y a t’il des progrès dans ce sens ?
Différents essais cliniques sont prévus ou en cours pour tester l’effet d’une alimentation enrichie en lipides. Il faut attendre le résultat de ces essais pour savoir avec certitude si l’on peut ralentir la progression de la maladie avec une intervention nutritionnelle. Pour les chercheurs, il nous faut comprendre l’origine des ces anomalies du métabolisme. L’élucidation des mécanismes nous permettra de disposer de cibles que nous pourrons atteindre avec des médicaments en complément, ou en remplacement, de régimes alimentaires spécifiques
Tu as publié récemment un article dans la revue Brain. Peux-tu nous dire quelques mots sur le lien entre sérotonine et SLA ?
Notre hypothèse de travail est que la disparition des neurones serotonergiques est un événement clé dans le développement des anomalies métaboliques. Nous testons actuellement cette hypothèse dans nos modèles de souris. Nous avons cependant déjà montré que la spasticité que certains patients développent pourrait aussi être une conséquence de la dégénérescence des neurones sérotonergiques. Cela pourrait avoir des conséquences à court terme pour le traitement de ce symptôme gênant et douloureux.
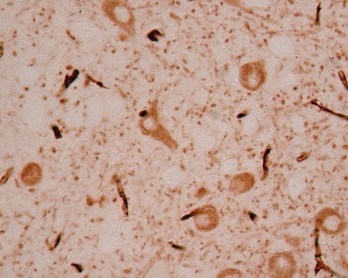
Figure 2 : Les travaux du Dr Luc Dupuis ont montré que les neurones sérotonergiques, en brun, présents dans le tronc cérébral, dégénéraient dans un modèle animal (ici en photo) et chez les patients atteints de SLA, provoquant notamment le développement de la spasticité.